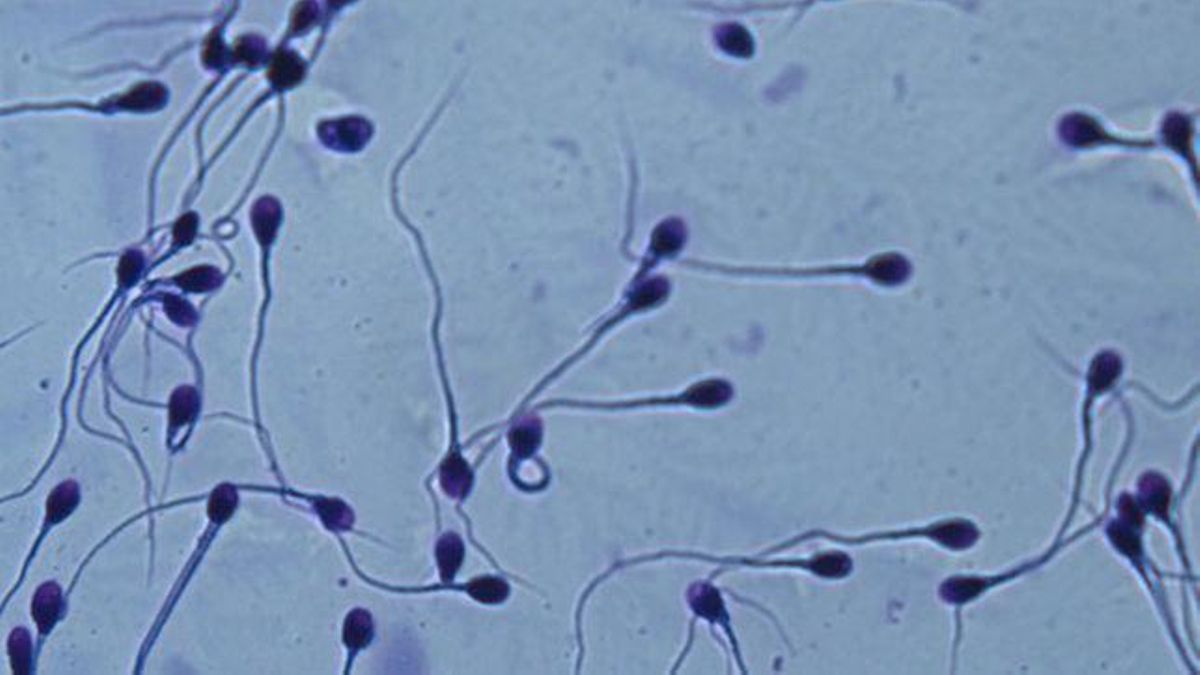
Logran reactivar el movimiento de espermatozoides paralizados y devolver la fertilidad a ratones estériles
Investigadores japoneses han conseguido restaurar, mediante terapia ARNm, la producción de esperma en ratones estériles y devolver la movilidad a espermatozoides paralizados. Ambos experimentos han culminado con el nacimiento de crías sanas
Hemeroteca – Consiguen por primera vez generar óvulos humanos potencialmente fecundables a partir de células de la piel
Utilizando la misma estrategia que las vacunas de ARNm contra la covid, un equipo de investigadores japoneses ha conseguido dar un prometedor paso en la lucha contra la infertilidad masculina. El equipo de Masahito Ikawa, de la Universidad de Osaka, ha logrado reactivar la producción de espermatozoides en ratones estériles y ha hallado una manera de restaurar su movilidad en determinados casos para que produzcan descendencia.
En un primer trabajo publicado este lunes en la revista PNAS, el equipo de Ikawa describe cómo han logrado restaurar la producción de esperma en animales que no podían producir gametos por un defecto genético. Mediante la inyección de ARNm y nanopartículas lipídicas (LNP) dirigidas a genes testiculares específicos, los autores lograron restaurar la producción de espermatozoides sanos y culminar el proceso con el nacimiento de descendencia viable.
Según los científicos, este resultado ofrece un enfoque innovador para el tratamiento de la infertilidad masculina causada por defectos genéticos. Al restaurar la espermatogénesis en un modelo de ratón con azoospermia no obstructiva con un gen muy concreto afectado, se introduce “una alternativa más segura y no integradora a las terapias génicas tradicionales, lo que brinda esperanza para los casos de infertilidad intratable en humanos”.
“El uso de LNP totalmente sintéticos para administrar ARNm minimiza los problemas de integración genómica y nos permite restaurar la espermatogénesis en un modelo genético definido”, subraya Ikawa. “Estos hallazgos aclaran cómo se puede recuperar la espermatogénesis y sientan las bases para la investigación aplicada en el tratamiento de ciertas formas de infertilidad masculina”, añade Martin M. Matzuk, coautor del artículo.
Espermatozoides que vuelven a nadar
En un segundo trabajo publicado en paralelo en la misma revista, el equipo de la Universidad de Osaka anuncia que también ha conseguido identificar y reactivar la proteína que actúa como el interruptor de movimiento en los espermatozoides. Al administrar un compuesto a los animales, los gametos volvieron a nadar y los científicos los usaron para fecundar un óvulo in vitro y producir el nacimiento de crías sanas.
Es un paso alentador hacia opciones prácticas para algunos tipos de infertilidad masculina
Para que los espermatozoides fecunden con éxito un óvulo, deben poder nadar, un proceso impulsado por su cola. Este movimiento es activado por una molécula de señalización esencial llamada AMP cíclico (AMPc), pero el mecanismo que lo regula sigue siendo un misterio. El equipo se centró en una proteína con una función previamente desconocida, la TMEM217, que se produce específicamente en los testículos.
Al modificar genéticamente a ratones para que no pudieran producir TMEM217, descubrieron que los machos eran completamente infértiles, con espermatozoides prácticamente inmóviles. Lo que han hecho es tomar los espermatozoides inmóviles de estos ratones y tratarlos con un análogo de la molécula que no funciona. Este tratamiento restauró con éxito la movilidad de los espermatozoides y les permitió fecundar óvulos in vitro, lo que resultó en el nacimiento de crías sanas. “Es un paso alentador hacia opciones prácticas para algunos tipos de infertilidad masculina”, dice Ikawa.
Combatir la azoospermia
Eduardo Roldán, investigador del MNCN-CSIC experto en biología molecular y reproducción, cree que ambos estudios son muy buenos y sus autores muy respetados en el campo. En el primero, apunta, restauran la producción de espermatozoides introduciendo en el testículo un ARN mensajero con las nanopartículas lipídicas. “La producción de espermatozoides se restaura transitoriamente, recuperan los espermatozoides y los usan mediante microinyección en los óvulos (ICSI). Después transfieren los embriones obtenidos y nacen crías que son fértiles”, resume.
“El método puede ser útil en el caso de varones que, por mutaciones, tienen azoospermia (ausencia de espermatozoides), ya que de esta manera repararían el proceso de formación de dichos espermatozoides”, observa el experto. “Sería de utilidad en los casos en que se pueda diagnosticar la causa (la mutación) que genera dicho trastorno”. Esto implica un pequeño porcentaje de los hombres estériles, alrededor de un 10 por ciento.
El método puede ser útil en el caso de varones que, por mutaciones, tienen azoospermia, ya que de esta manera repararían el proceso de formación de los espermatozoides
Por otro lado, es importante señalar que el tratamiento con ARNm no cura la esterilidad del ratón, ya que no corrigen la mutación (de hecho resaltan que el método no lleva a una modificación del ADN). “La corrección es transitoria y la descendencia masculina podría tener el mismo problema”, asegura.
En el segundo trabajo, apunta Roldán, los autores tienen un ratón que produce espermatozoides pero que son inmótiles (no se mueven). “En este caso restauran la motilidad con un compuesto que actúa en la vía de señalización por debajo de lo que está dañado. Estos espermatozoides tratados son capaces de fecundar, en este caso usando fecundación in vitro y los embriones transferidos dan origen a una cría”. “Ambos trabajos son parte de las líneas de investigación del grupo de Masahito Ikawa que apunta a identificar genes que son importantes en espermatogénesis y en la función espermática, utilizando un abanico de herramientas”, concluye Roldán.
Esperanza con cautela
Meritxell Jodar, especialista en biología molecular de la reproducción del Hospital Clínic, cree que se trata de dos trabajos muy interesantes, pero pide cautela a la hora de interpretarlos, ya que en fertilidad los resultados en ratones son particularmente difíciles de traducir a humanos. “Me parece brillante, como prueba de concepto, el tratamiento con ARNm, pero si se trasladara a personas habría que personalizarlo para cada paciente, porque cada uno puede tener el problema en un gen diferente, aparte de que sería invasivo y doloroso, y aún no sabemos si seguro”, explica.
Me parece brillante, como prueba de concepto, el tratamiento con ARNm, pero si se trasladara a personas habría que personalizarlo para cada paciente
Jodar admira el trabajo Ikawa, que tiene una colección de ratones con mutaciones en casi todos los genes que afectan a la infertilidad masculina, y ahora está dando un paso más allá para tratar de desarrollar posibles tratamientos. “Es un esfuerzo valioso avanzar en el conocimiento de estas causas, porque tradicionalmente la infertilidad en los hombres se ha estudiado menos”, comenta a elDiario.es. “Pero la falta de producción de espermatozoides es una de las condiciones más multifactoriales que puede haber, y tendremos que ir a una medicina personalizada; no creo que encontremos nunca un medicamento que pueda ayudar a un 40% de pacientes, por ejemplo, porque se produce de muchas maneras diferentes”.


